日前,国际生物医学重要期刊Autophagy(《自噬》影响因子12.04)在线发表了附属瑞金医院神经病学研究所乐卫东教授研究组题为“MTOR非依赖自噬激活剂海藻糖通过调控体内自噬通量保护肌萎缩侧索硬化症(ALS)模型小鼠的存活”
的研究论文。该项研究在前期工作的基础上,国际上首次提出了ALS中自噬通量异常是ALS发病的一个新机制,并将目标集中于自噬小体与溶酶体融合过程,为ALS的治疗新靶点提供了理论依据。
据介绍,ALS是最为常见的一种成人运动神经神经元疾病,至今缺乏特异的治疗药物,以往的研究已发现运动神经元内蛋白质的异常累积可能在其选择性退行性变过程中起重要作用;自噬和蛋白酶体是胞内蛋白质降解的两条主要途径,其中自噬主要负责降解聚集状蛋白质。乐卫东课题组前期研究报道了ALS中自噬水平的异常增高,而其在疾病发生发展过程中的作用及机制尚未阐明。
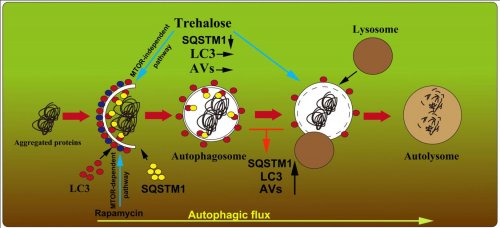
上图为自噬在肌萎缩侧索硬化发病中的作用及海藻糖作用靶点示意图
在乐卫东教授的指导下,博士研究生张晓洁和陈晟等利用SOD1-G93A模型小鼠,首次发现并报道了ALS中自噬通量的异常,尤其是自噬小体与溶酶体的结合过程出现障碍;进而发现MTOR非依赖自噬激活剂海藻糖能够通过促进自噬小体与溶酶体的融合,加速聚集状蛋白质的降解,从而保护运动神经元的存活,延缓疾病的发生发展。同时,研究发现海藻糖还具有保护线粒体功能,延缓ALS骨骼肌的退化,对抗凋亡发生等多种神经保护作用。该研究还发现ALS的发生与运动神经元内自噬通量异常密切相关,而MTOR非依赖自噬激活剂海藻糖能够改善自噬通量,保护运动神经元,显著延长模型小鼠的生存时间。
课题组进一步的研究发现,海藻糖对ALS中自噬通量的改善及其在模型小鼠中的神经保护作用,其可能为临床ALS的治疗潜在药物。此外,研究结果对以胞内蛋白聚集为特征的其他神经退行性疾病如帕金森症、阿尔茨海默症的发病机制研究和潜在的治疗新靶点也提供了积极的借鉴意义。
此课题得到了国家自然科学基金,科技部973项目及教育部博士点基金的资助。

